Муковисцидоз: определение, диагностические критерии, терапия. Национальный консенсус - Страница 18
Таким образом, при анализе микрофлоры больных МВ можно утверждать, что с увеличением возраста у больных формируются постоянные очаги хронической легочной инфекции, основными возбудителями которой являются P. aeruginosa и S. aureus.
Особенностью бактерий P. aeruginosa, S. aureus и Bcc, Achromobacter spp. является устойчивость ко многим антибиотикам.
4.1. Микробиологические свойства основных возбудителей хронической респираторной инфекции при муковисцидозе
Микроорганизмы, инфицирующие больного МВ, определяют лечение, качество жизни, перспективы для трансплантации и общую выживаемость. Точная и своевременная идентификация возбудителей инфекций дыхательных путей имеет существенное значение для обеспечения своевременного начала лечения соответствующими антибиотиками в целях элиминации бактериальных патогенов и организации надлежащего инфекционного контроля для профилактики распространения патогенных микроорганизмов среди больных МВ. Ниже приведены основные микробиологические характеристики доминирующих возбудителей хронической респираторной инфекции и представлен алгоритм ее микробиологической диагностики.
Staphylococcus aureus
В настоящее время род Staphylococcus, относящийся к семейству Micrococcus, включает 45 видов [8]. Вид S. aureus – золотистый стафилококк – является одним из значимых патогенов для пациентов с МВ. Он вызывает хроническую инфекцию легких, приобретаемую в обществе и во время лечения в госпитальных условиях [9].
Бактерии S. aureus представляют собой грамположительные неподвижные кокки, при микроскопии располагающиеся в виде характерных скоплений – гроздей. Стафилококки не образуют спор, но могут образовывать капсулы. У больных МВ могут выделяться 3 морфологических типа колоний – мукоидные, немукоидные и с SCV (small-colony varients)-фенотипом [9]. SCV-фенотип представляет собой мелкие, без гемолиза и пигмента, медленно растущие колонии на 5% кровяной и шоколадной плотных агаризованных средах.
Особое значение для больных МВ имеют метициллин-устойчивые стафилококки (MRSA), которые обладают устойчивостью ко многим антибиотикам. МRSA обнаруживаются во многих больницах большинства стран мира. MRSA распространяются от человека к человеку, обычно с рук медперсонала [23]. Однако могут встречаться и другие механизмы передачи, например воздушно-капельный. Некоторые штаммы являются чрезвычайно трансмиссибельными, распространяясь внутри палат, между палатами и из больницы в больницу [23].
Неферментирующие грамотрицательные микроорганизмы
Среди возбудителей хронической инфекции легких у больных МВ значимое место занимают НФМО, общими признаками которых являются природная устойчивость ко многим антибиотикам, высокая резистентность к дезинфектантам и распространение в больничных стационарах от больного к больному [10]. НФМО, наиболее часто вызывающие инфекции, принадлежат к нескольким родам и условно могут быть разделены на оксидазоположительные – роды Pseudomonas (кроме видов P. luteola и P. oryzihabitans), Burkholderia, Moraxella, Chryseobacterium – и оксидазоотрицательные – роды Stenotrophomonas, Acinetobacter, Bordetella (кроме B. pertussis, B. avium, B. bronchiseptica, B. hinzii) [11-13].
Большинство из упомянутых выше родов и видов НФМО обладают высокой степенью фенотипического и генотипического родства с бактериями рода Pseudomonas, и многие из них еще в 90-х гг. прошлого века относились к данному роду. Все эти микроорганизмы могут быть выделены из окружающей среды, однако клинической значимостью характеризуются только отдельные виды некоторых родов.
Pseudomonas aeruginosa
Первоначальная классификация рода Pseudomonas, состоящего из пяти соответствующих rRNA-групп, подверглась радикальному пересмотру, закончившемуся изменением классификации многих видов рода Pseudomonas и объединением в отдельные роды. Эти роды включают Burkholderia, Stenotrophomonas, Comamonas, Shewanella, Ralstonia, Methylobacterium, Sphingomonas, Acidovorax и Brevundimonas. Род Pseudomonas (sensu stricto) включает соответствующую rRNA-группу 1 и объединяет 11 видов: Pseudomonas aeruginosa, P. fluorescens, P. putida, P. veronii, P. monteilii, P. stutzeri, P. mendocina, P. pseudoalcaligenes, P. alcaligenes, P. luteola, P. oryzihabitans.
Псевдомонады являются аэробными неспорообразующими грамотрицательными палочками, которые могут быть прямыми или слегка изогнутыми. Они имеют от 1,5 до 5 мкм в длину и от 0,5 до 1,0 мкм в ширину и обладают строгим дыхательным метаболизмом с использованием кислорода как конечного акцептора электронов. Некоторые изоляты могут расти в анаэробных условиях с использованием нитратов или аргинина в качестве конечных акцепторов электронов. Псевдомонады подвижны благодаря присутствию одной или более полярных флагелл. Клинические изоляты являются оксидазоположительными (за исключением P. luteola, P. oryzihabitans) и каталазоположительными, а также растут на агаре МакКонки как лактозонегативные колонии [12].
Псевдомонады широко распространены в природе с преимущественным обитанием в окружающей среде, связанной с водой. Они обнаружены в воде, почве, на растениях, включая овощи и фрукты. Ввиду способности выживать в водной среде эти микроорганизмы, особенно P. aeruginosa, стали одной из основных проблем в качестве возбудителей госпитальных инфекций [12]. Бактерии P. aeruginosa являются ведущей причиной нозокомиальных инфекций дыхательного тракта. Особое значение имеют для больных МВ. Основную роль в патогенезе инфекции легких у больных МВ играют мукоидный фенотип P. aeruginosa и воспалительные реакции больного [1, 9, 14].
Бактерии Burkholderia cepacia complex (Bcc)
Бактерии Bcc – это группа грамотрицательных, неспоробразующих бактерий. В мазках, окрашенных по Граму, эти микроорганизмы представляют собой полиморфные прямые грамотрицательные палочки размером 0,5-1,0 х 1,5-5 мкм. После культивирования на 5% кровяном агаре при t = 30 °C в течение 48 ч бактерии Bcc образуют серые гладкие колонии с ровными краями размером 1-2 мм с резким характерным запахом гнили. При наличии пигмента колонии могут быть окрашены в желтый цвет различной интенсивности. Вокруг колоний могут образовываться зоны гемолиза. На средах Эндо и МакКонки колонии Bcc размером 1 мм окрашены в светло-розовый цвет (лактозонегативные).
В настоящее время вид B. cepacia sensu lato включает 20 близкородственных геномоваров.
Таблица 1. Представители Burkholderia cepacia complex
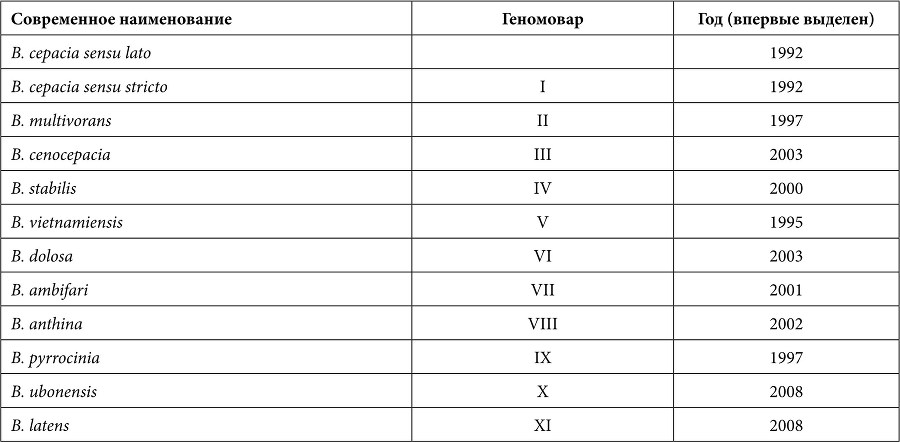

Все геномовары могут выделяться от больных МВ, однако преобладающим является геномовар III – B. cenocepacia, обнаруженный в 70% случаев инфекции, вызванной Bcc, в Англии, Бельгии, США, Канаде [15].
В России от больных МВ, а также при исследовании образцов от больных с пневмонией в отделениях интенсивной терапии различных клиник города Москвы также были выявлены бактерии Bcc, преимущественно принадлежащие к геномовару IIIA – B. cenocepacia [14, 16].
Клиническое значение бактерий Bcc и патогенез вызванной ими инфекции
О колонизации легких Bcc у больных МВ впервые сообщено в начале 1970-х гг. [38]. Приблизительно у 20% больных, колонизированных Bcc, возникал так называемый «сепация-синдром», характеризующийся некротизирующей пневмонией с лихорадкой, бактериемией, увеличением СОЭ и лейкоцитозом, который приводил к быстрому летальному исходу. Было высказано предположение, что появление Bcc является основной причиной неблагоприятного исхода у больных МВ. В настоящее время установлено, что Bcc представляет особую опасность для больных МВ. Хроническая микробная колонизация дыхательных путей ведет к развитию легочной инфекции – основной причины прогрессирования бронхолегочного процесса и смертности у больных МВ. Установлено, что особенностью инфекции при МВ является персистенция ассоциаций микроорганизмов в 59,4% случаев. Особенностью персистенции штаммов Bcc является тяжелое течение в виде смешанной инфекции в ассоциации с бактериями P. aeruginоsa. Бактерии Bcc, способные персистировать у больных МВ, характеризуются устойчивостью ко многим антибиотикам. Доказана длительная (до 1 года 5 мес) персистенция штаммов Bcc, выделенных от одного больного, с помощью мониторинга микрофлоры НДП. Штаммы Bcc, колонизируя НДП больных МВ, способны длительно персистировать и передаваться от пациента к пациенту [3, 17, 18].